Ангина при лейкозе
Содержание статьи
Ангина при лейкозе — вариант острого тонзиллита, развивающийся на фоне злокачественного перерождения клеток костного мозга. Основные проявления — пиретическая лихорадка, последовательное развитие катаральных, гнойных, язвенно-некротических изменений небных миндалин, лимфаденопатия в сочетании с общим иммунодефицитом, анемией и геморрагическим синдромом. Для постановки диагноза используются анамнестические сведения, жалобы пациента, результаты фарингоскопии, общего анализа крови и пункции костного мозга. В программу лечения входят массивная антибактериальная терапия, химиотерапия, гемотрансфузии и трансплантация костного мозга.
Общие сведения
Ангина — одно из патогномоничных проявлений как острого, так и хронического лейкоза. При острых формах лейкоза поражение небных миндалин возникает у 35-95% больных; примерно у трети пациентов выступает одним из первых и ранних признаков лейкемии. Хронические формы сопровождаются развитием ангины несколько реже — в 20-25% случаев. Острые лейкозы характерны для детей и лиц в возрасте до 30 лет, в то время как хронический вариант чаще наблюдается у людей старшего возраста. Согласно статистическим данным, заболевание более распространено среди мужчин. Сезонных и географических особенностей эпидемиологии не прослеживается.
Ангина при лейкозе
Причины ангины при лейкозе
Основным этиологическим фактором является группа онкогематологических заболеваний — острые и хронические лейкозы (лейкемии). Это злокачественные опухоли костного мозга, для которых характерно образование очагов патологического гемопоэза и неспособность продуцировать полноценные зрелые форменные элементы крови. Зачастую пусковым фактором развития ангины при лейкозе является минимальное нарушение целостности слизистой оболочки ротовой полости или миндалин. В норме лимфатическое глоточное кольцо постоянно контактирует с большим количеством патогенной микрофлоры и успешно противостоит ей. Но при лейкозе резко снижается общий и местный иммунитет, что проявляется выраженной склонностью к воспалительным и некротическим процессам. Поэтому посещение стоматолога, профилактический осмотр отоларинголога или любое случайное повреждение может привести к проникновению бактерий внутрь тканей и быстрому развитию ангины.
Патогенез
При лейкозе этиологический агент вызывает мутацию гемопоэтических клеток I-III класса. Образовавшиеся злокачественные клетки-предшественники лимфопоэза активно взаимодействуют с ростовыми факторами, чем угнетают нормальные процессы дифференциации. Таким образом, костный мозг теряет способность продуцировать эритроциты, лейкоциты и тромбоциты. Вместо них в периферическую кровь попадает большое количество низкодифференцированных клеток-бластов. Это проявляется выраженным иммунодефицитом, анемическим и геморрагическим синдромами, лейкемической инфильтрацией лимфоидной и других тканей организма. Отсутствие общего иммунного ответа, местное снижение реактивности и резистентности небных миндалин и повреждение слизистых оболочек дает возможность патогенной микрофлоре бесконтрольно размножаться в тканях ротовой полости. Активная жизнедеятельность бактерий на фоне инфильтрации лейкоцитами быстро приводит к выраженным воспалительным и некротическим изменениям, которые обуславливают последовательное развитие различных форм ангины.
Симптомы ангины при лейкозе
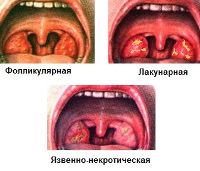
Более чем в половине случаев поражению небных миндалин предшествуют другие симптомы лейкемии. Они включают в себя общую слабость, боль в костях, субфебрилитет, мелкоточечную геморрагическую сыпь на конечностях. Даже при минимальных повреждениях кожи или слизистых оболочек возникают длительные кровотечения. Поражение миндалин чаще всего возникает на 3-5 сутки после первичного проявления лейкоза или его рецидива и характеризуется последовательным развитием катаральной, лакунарной или фибринозной и язвенно-некротической ангины.
Катаральная ангина при лейкозе проявляется выраженным отеком слизистой оболочки рта, увеличением небных миндалин, повышением температуры тела до 39-40ОС. Клинически это сопровождается болью и дискомфортом при глотании, чувством инородного тела в горле, ознобом, потливостью. Параллельно возникает гиперплазия подбородочных, нижнечелюстных и шейных групп лимфатических узлов. Реже наблюдается их болезненность и изменение консистенции. Для хронического лимфолейкоза характерна выраженная генерализованная лимфаденопатия, для миелолейкоза — значительное увеличение печени и селезенки.
Спустя 1-3 дня после возникновения первых симптомов катаральной ангины происходит ее трансформация в лакунарную или фибринозную форму. Это сопровождается развитием выраженного интоксикационного синдрома, болями в суставах и пояснице. Боль в горле значительно усиливается, может возникать иррадиация в ухо. Спустя 24-48 часов изменения небных миндалин приобретают характер язвенно-некротических и распространяются на слизистые оболочки десен, зева, глотки. Общее состояние больного прогрессивно ухудшается, а ранее имеющиеся симптомы дополняются гнилостным запахом изо рта и повышенным слюноотделением. Развитие язвенно-некротической ангины свидетельствует о злокачественном течении лейкоза.
Осложнения
Осложнения, которые возникают при ангине на фоне лейкоза, обусловлены иммунодефицитом, лейкемической инфильтрацией и тромбоцитопенией. Отсутствие функционально активных лейкоцитов способствует быстрому распространению инфекции. Не начатая своевременно антибактериальная терапия приводит к развитию сепсиса и инфекционно-токсического шока — одних из наиболее частых причин смерти при лейкозах. Дефицит тромбоцитов способствует ухудшению свертываемости крови, спонтанным внешним и внутренним кровотечениям. Также характерно поражения легких и оболочек мозга в виде лейкемических пневмоний и нейролейкоза.
Диагностика
Диагностика основывается на выявлении местных симптомов острого тонзиллита в комбинации с клинико-гематологическими проявлениями лейкоза. Постановка диагноза осуществляется совместно отоларингологом и гематологом. Как правило, в диагностическую программу входят:
- Сбор анамнеза и жалоб. Наличие анемического и геморрагического синдрома, помимо классических проявлений ангины, указывает на сопутствующее нарушение гемопоэза. Часть пациентов с ранее установленной лейкемией сами сообщают об этом в момент обращения к врачу.
- Фарингоскопия. Определяемые изменения зависят от формы ангины, которая имеется у пациента на момент осмотра. Катальный тонзиллит проявляется отеком, гиперплазией и гиперемией небных миндалин. Лакунарная форма характеризуется белыми или желтыми налетами, которые легко отделяются от подлежащих тканей. При фибринозном варианте эти налеты полностью покрывают миндалины и переходят на окружающие ткани. Язвенно-некротическая ангина при лейкозе проявляется образованием участков бурого и грязно-серого цвета по всей ротовой полости и глотке. На месте отторжения отмерших тканей формируется глубокий, обильно кровоточащий дефект.
- Общий анализ крови. При исследовании крови выявляется снижение уровня эритроцитов до 1,0-2,0×1012/л, гемоглобина ниже 50 г/л, тромбоцитов ниже 100×109/л, повышение СОЭ. Уровень лейкоцитов зависит от формы заболевания и может колебаться в пределах от 0,5×109/л до 50×109/л и выше. Характерный признак лейкоза — наличие в крови бластных клеток (гемогистиобластов, миелобластов, лимфобластов), которые составляют до 95% всех выявленных форменных элементов.
- Стернальная пункция. В миелограмме определяется большое количество бластов (более 30% всех клеток) на фоне выраженной редукции клеток эритроидного, гранулоцитарного и мегакариоцитарного ростков.
Дифференциальная диагностика проводится с дифтерией, классическим острым тонзиллитом и агранулоцитарной ангиной. Основное отличие всех вышеупомянутых заболеваний от ангины при лейкозе — отсутствие большого количества бластных клеток в периферической крови и пунктате костного мозга.
Лечение ангины при лейкозе
Терапевтическая тактика сводится к борьбе с язвенно-некротическим поражением небных миндалин, слизистых оболочек и лечению лейкоза. Для местного воздействия на поврежденные ткани показаны полоскания ротовой полости антисептическими растворами и орошения масляными растворами витаминов. Также в терапевтическую программу входят:
- Антибиотикотерапия. Антибиотики подавляют патогенную микрофлору, предотвращают развитие других септических осложнений. Используются антибактериальные средства широкого спектра действия, комбинации препаратов различных классов: пенициллинов, аминогликозидов, цефалоспоринов.
- Схемы полихимиотерапии (ALL-BFM-2000, ALL IC-BFM-2002 и другие). В их состав входят фармакологические препараты с различным механизмом действия. Такие комбинации позволяют одновременно воздействовать на разные фазы митоза раковых клеток, тем самым добиваться их угнетения и эрадикации.
- Лучевая терапия. Использование радиационного излучения дает возможность противодействовать опухоли без нанесения существенного вреда костному мозгу. Это обусловлено высокой митотической активностью злокачественных клеток, что повышает их чувствительностью к излучению.
- Гемотрансфузии. Переливание эритроцитарной, тромбоцитарной и лейкоцитарной массы позволяет временно компенсировать недостаток форменных элементов крови больного и корректировать связанные с этим нарушения.
- Дезинтоксикационная терапия. Внутривенное введение дезинтоксикационных препаратов снижает концентрацию токсических веществ и ускоряет их выведение из организма. При необходимости могут использоваться экстракорпоральные методы детоксикации: плазмаферез, гемосорбция и плазмосорбция.
- Трансплантация костного мозга. Пересадка донорской костномозговой ткани позволяет обогатить костный мозг больного человека здоровыми гемопоэтическими клетками и восстановить синтез полноценных форменных элементов.
Прогноз и профилактика
Прогноз для больных с ангиной при лейкозе неблагоприятный. В первые 1-2 месяца смертность составляет 75%. Однако этот показатель напрямую зависит от своевременности и правильности терапевтических мероприятий. Основные причины смерти — системные септические осложнения и внутренние кровоизлияния. Специфической профилактики развития ангины при лейкозе не разработано. К неспецифическим превентивным мерам относятся полоскание ротовой полости растворами антисептиков, лекарственная обработка миндалин и задней стенки глотки, соблюдение масочного режима при контакте больного с окружающими, профилактическое употребление антибиотиков и рациональное лечение лейкоза.
Источник
ЛЕЙКОПЕНИЯ
Лейкопения (leukopenia; греч. leukos белый + penia бедность; син. лейкоцитопения) — уменьшение количества лейкоцитов в крови (менее 4000 в 1 мкл). Обычно Лейкопения обусловлена снижением содержания нейтрофилов (гранулоцитопенией, правильнее — нейтропенией).
Этиологические факторы Лейкопении разнообразны. К развитию Лейкопении приводят некоторые физические воздействия (ионизирующее излучение), контакт с рядом химических агентов (бензолом, мышьяком, ДДТ и др.), прием многих медикаментозных препаратов (цитостатических средств, некоторых антибиотиков, сульфаниламидов, антитиреоидных препаратов и др.). Л. нередко возникает при вирусных и тяжело протекающих бактериальных инфекциях, малярии, некоторых коллагенозах. Л.- закономерный гематол, симптом многих заболеваний системы крови, напр. В12-(фолиево) дефицитной и гипопластической анемии, пароксизмальной ночной гемоглобинурии и др. С лейкопенией протекают многие заболевания, сопровождающиеся увеличением селезенки (портальный цирроз, синдром Фелти, брюшной тиф и др.), а также острые анафилактические реакции. Выделяется большая группа Л. невыясненной этиологии.
Патогенез лейкопении различен и зависит от причин, вызвавших ее. Лейкопения может быть обусловлена уменьшением продукции лейкоцитов, нарушением выхода зрелых нейтрофилов из костного мозга, ускоренным разрушением лейкоцитов, перераспределением лейкоцитов в сосудистом русле, ускоренным выведением лейкоцитов из циркуляции, сочетанием нескольких патогенетических механизмов. Уменьшение продукции нейтрофилов может быть вызвано нарушением способности родоначальных клеток дифференцироваться в гранулоцитарные элементы (патологией родоначальных клеток, микроокружения или дефицитом факторов, регулирующих гранулоцитопоэз), нарушением созревания собственно гранулоцитарных элементов (блоком созревания), усиленным разрушением лейкоцитарных элементов в костном мозге (неэффективным гранулоцитопоэзом), вытеснением гранулоцитарных элементов патологическими клетками (метастазами опухоли, лейкемической инфильтрацией). Л. лучевая (радиационная) может возникать при воздействии как общего, так и местного облучения. Она обусловлена торможением пролиферативной активности кроветворных клеток, в т. ч. и родоначальных клеток, с уменьшением продукции всех видов лейкоцитов. Меньшее значение в возникновении Л. имеет непосредственное лейкоцитолизирующее действие облучения, наиболее четко проявляющееся в отношении лимфоцитов (см. Кроветворение, патология).
Лейкопения, связанная с нарушением выхода зрелых нейтрофилов из костного мозга в кровь, обусловлена резким торможением их двигательной активности (синдром «ленивых лейкоцитов»).
Лейкопения при ускоренном разрушении лейкоцитов возникает в тех случаях, когда костный мозг не в состоянии компенсировать распад лейкоцитов. Ускоренное разрушение лейкоцитов отмечается при иммунной Л., обусловленной появлением антител к лейкоцитам (чаще лейкоагглютининов). Обычно иммунная Л. развивается при приеме амидопирина и его производных у лиц, сенсибилизированных к этим препаратам. В этих случаях препарат (гаптен) соединяется с молекулой белка и организм вырабатывает антитела, направленные на сложный антигенный комплекс. Антитела могут взаимодействовать с антигеном в крови с последующей адсорбцией комплекса на поверхности лейкоцитов. Препарат может вступать в соединение с белками оболочки лейкоцитов, может происходить и фиксация антител на поверхности лейкоцитов при свободной циркуляции антигена. Врожденная изоиммунная Л. обычно обусловлена антигенной несовместимостью лейкоцитов матери и плода. Антитела могут воздействовать не только на циркулирующие в крови лейкоциты, но и на гранулоцитарные элементы костного мозга из-за близости их антигенной структуры.
При спленомегалии ускоренное разрушение лейкоцитов приводит к развитию Л. В этих условиях значительное количество лейкоцитов депонируется в увеличенной селезенке с последующим их фагоцитозом.
В основе перераспределительной Л. лежит нарушение равновесия между свободно циркулирующими лейкоцитами (циркулирующий пул) и лейкоцитами, занимающими краевое положение в сосудистом русле (так наз. депонированные лейкоциты, или маргинальный пул). Увеличение числа лейкоцитов в маргинальном пуле отмечается при анафилактическом шоке, спленомегалии, хронических воспалительных заболеваниях жел.-киш. тракта, ваготонии, а также при проведении гемодиализа.
В зависимости от длительности существования выделяют острые, хронические, рецидивирующие и циклические Л. Описаны врожденные и наследственные Л.
Клин, проявления Лейкопении определяются ее выраженностью и степенью изменений функциональной активности гранулоцитов. При снижении абсолютного числа зрелых нейтрофилов до 800 в 1 мкл клин, проявления отсутствуют. При более низких цифрах возможно развитие инфекционно-воспалительных заболеваний. Изменения функц, активности лейкоцитов, способствующие развитию воспалительных осложнений, наиболее выражены при Л., обусловленной нарушениями продукции лейкоцитов (угнетением фагоцитарной активности из-за нарушений внутриклеточного метаболизма). При перераспределительной Л. функц, активность лейкоцитов не изменена (доброкачественная Л.).
При наличии у больного Л. причину ее устанавливают по данным анамнеза. Результаты клин, и лаб. исследования позволяют исключить симптоматическую Л., связанную с наличием основного патол, процесса. Наконец, для уточнения вопроса о причине Л. необходимо проведение специальных исследований. Диагноз Л. костномозгового генеза подтверждается при изучении миелограмм (см.) и срезов костного мозга (см. Трепанобиопсия). Определенную ценность для выяснения патогенеза Л. представляет изучение кинетики нейтрофилов, способности гранулоцитарных элементов костного мозга утилизировать предшественники синтеза нуклеиновых к-т в культурах, а также культивирование костного мозга в полутвердых агаровых средах для оценки его колониеобразующей способности (см. Культуры клеток и тканей). Диагноз аутоиммунной Л. в отдельных случаях удается подтвердить соответствующими иммунол, тестами (выявление лейкоагглютининов, лейколизинов и др.). Перераспределительная Л. может быть подтверждена при проведении тестов с соединениями, вызывающими переход лейкоцитов из краевого в циркулирующий пул (пробы с адреналином, эфедрином). Истощение костномозгового резерва гранулоцитов выявляется пирогеналовой пробой. Л., обусловленная воздействием ионизирующего излучения, может быть подтверждена хромосомным анализом лимфоцитов периферической крови и костного мозга.
Врачебная тактика при Л. определяется ее этиологией, патогенезом и выраженностью клин, проявлений. Необходимо устранить причину, вызвавшую Л., напр, запретить прием соответствующих медикаментозных препаратов. При Л., обусловленной нарушениями гранулоцитопоэза, используются андрогены и препараты анаболического действия, витамины, а при наличии воспалительных осложнений — антибиотики. Для лечения аутоиммунной Л. обычно применяют глюкокортикоиды, а по специальным показаниям — другие иммунодепрессоры (см. Иммунодепрессивные вещества) или же спленэктомию (см.). Хрон. Л. селезеночного генеза ликвидируется после спленэктомии, к-рая производится при наличии других показаний (портальная гипертензия, геморрагический диатез и др.). Больные с перераспределительными Л. не нуждаются в специальной терапии .
Профилактика Лейкопении сводится к запрещению бесконтрольного приема медикаментов, обладающих лейкопеническим действием, соблюдению гигиенических нормативов на соответствующих предприятиях, а также своевременному лечению заболеваний, обусловливающих развитие Л.
Особенности лейкопении у детей
Количество лейкоцитов у детей имеет выраженную возрастную зависимость, поэтому Л. следует считать снижение количества лейкоцитов более чем на 30% от средневозрастной нормы (см. Кровь). Врожденные формы Л. могут быть генетически обусловленными или развиваться вследствие антигенной несовместимости лейкоцитов матери и плода, приема женщиной во время беременности различных медикаментов, наличия профвредностей, воздействия ионизирующего излучения и других причин. Лейкоциты обладают монотканевыми и политканевыми антигенами. Вследствие антигенной несовместимости лейкоцитов матери и плода наблюдается изоиммунная Л. новорожденных детей. Изоагглютинины матери свободно переходят через плаценту к плоду. В случае монотканевой антигенной несовместимости изоагглютинины активны в отношении гранулоцитов. Монотканевые изоагглютинины, вызывающие Л. у новорожденных, сохраняются в течение 6 -12 нед. Наиболее изучены у новорожденных нейтропении, обусловленные изоиммунизацией. Они имеют латентное или клинически выраженное течение. Диагноз изоиммунной Л. иногда подтверждается реакцией лейкоагтлютинации (см. Агглютинация). Наряду с изоиммунной Л. у новорожденных могут наблюдаться Л., обусловленные трансплацентарной передачей других, еще недостаточно изученных факторов, напр, скоропреходящая Л. у новорожденных от матерей с диссеминированной красной волчанкой.
Врожденные формы лекарственной Лейкопении, обусловленной гиперсенсибилизацией к лекарственным препаратам, у новорожденных объясняются трансплацентарной передачей антител от матери к плоду. Если имеется генетически детерминированная непереносимость, то Л. развиваются у детей после рождения и выявляются при назначении соответствующих медикаментов. Удается установить непереносимость одних и тех же препаратов в семье. Приобретенная форма лекарственной Л. развивается лишь при повторном приеме одних и тех же медикаментов. Клин, проявления лекарственной Л. могут значительно варьировать — от латентной, выявляемой при лаб. исследовании крови, до тяжелых панцитопений; при этом наблюдаются гипо- и аплазия костного мозга вследствие сходной антигенной структуры элементов, находящихся на разных стадиях созревания.
Реже наблюдается Л. за счет снижения количества лимфоцитов-лимфопения при врожденных иммунодефицитных заболеваниях тимусного генеза.
Течение Л. у детей может быть острым, подострым и хроническим. Острые и подострые формы Л. при уменьшении количества нейтрофилов до 750-500 в 1 мкл (агранулоцитоз) обусловливают развитие генерализованной инфекции нередко с неблагоприятным исходом. Хронические формы Лейкопении имеют перманентное или волнообразное течение. Среди Л. следует выделить так наз. невинную Л. (leucopenia innocens), являющуюся, по мнению И. А. Кассирского, одним из вариантов физиол, нормы и обусловленную перераспределением лейкоцитов в организме. При этой Л. костномозговое кроветворение нормальное; не выявляется отклонений в функциональных свойствах лейкоцитов; резервы лейкоцитопоэза не нарушены; лечения не требуется.
Библиография: Доссе Ш. Иммуногематология, пер. с франц., М., 1959; Истаманова Т. С., Алмазов В. А. и Канаев С. В. Функциональная гематология, Л., 1973, библиогр.; Кассирский И. А. и Денщикова Д. И. Физиологические нормы лейкоцитов и проблема leucopenia innocens, М., 1974, библиогр.; Лавкович В. и Кржеминьска-Лавкович И. Гематология детского возраста, пер. с польск., с. 215, Варшава, 1964; Barnes R. D. a. Tuffrey M. Maternal cells in the newborn, Advanc. Biosciences, v. 6, p. 457, 1971; Cline M. The white cell, Cambridge, 1975; Gitlin D., Vawter G. a. Craig J. M. Thymic alymphoplasia and congenital aleukocystosis, Pediatrics, v. 33, p. 184, 1964; Greenberg P. L. a. Schrier S. L. Granulopoiesis in neutropenic disorders, Blood, v. 41, p. 753, 1973, bibliogr.
В. А. Алмазов; А. В. Мазурин (пед.).
Источник